2014.07.07 より
寒天ゲル中の炭酸カルシウムの結晶生成 その2 [ゲル中結晶]
前回に引き続きであるが、今度は塩化アンモニウムの代わりに塩化マグネシウムを共存させる作戦だ。
塩化アンモニウムを共存させる所以は、この物質が炭酸カルシウム(もしくは炭酸水素カルシウム)の水への溶解を助けるゆえ、炭酸カルシウムの結晶生成速度を抑えることが出来るという期待からである。
これに対して、何故、塩化マグネシウムを代替することを思いついたかというと、まず予想に反してこの系で炭酸マグネシウムの沈殿が出来ないことだ。
この辺はよくわからないが、中性付近では炭酸水素マグネシウムができ、これが水に溶けやすいからだと思う。
そしてもう一点は、塩化アンモニウムと同様、炭酸カルシウムの沈殿が生じているところに塩化マグネシウムを加えると沈殿が溶解することを確かめたからである。
その他は前回の条件と同様にして、次のような実験だ。
実験 5 寒天 0.5% ゲル
実験 6 寒天 0.3% ゲル
実験 7 寒天0.1%+ゼラチン2% ゲル
実験 8 イナアガーA 2% ゲル
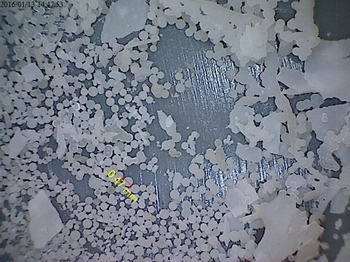
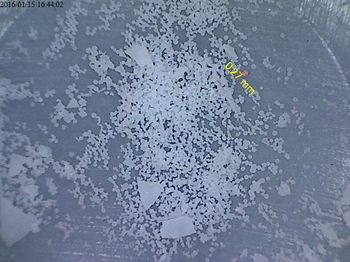
写真を見ればもう説明はいらない。
まず、結晶は球晶が主だということ。
小さいこと。
ゲルとの関連からいえば、結晶は小さいものの、大きさの傾向は前回と同様だった。
結論から言えば、大きな結晶を作るためにやったことだが、より小さな結晶を作ってしまったということだ。
まあ、思いつきが見事に外れたの巻だ。
まあ自分の傾向として、思いつきの時は、いい着想だと自賛してわくわくし、その結果が楽しみで外れのことなんかあまり考えないのだが、外れがわかると何でこんなことしたんかとがっかりし、もう見るのもイヤになる。
しかし、外れでもまとめることはしないといかん。
誰が読んでくれてるかは知らんが、ブログはそのモチベーションにはなる。
塩化アンモニウムを共存させる所以は、この物質が炭酸カルシウム(もしくは炭酸水素カルシウム)の水への溶解を助けるゆえ、炭酸カルシウムの結晶生成速度を抑えることが出来るという期待からである。
これに対して、何故、塩化マグネシウムを代替することを思いついたかというと、まず予想に反してこの系で炭酸マグネシウムの沈殿が出来ないことだ。
この辺はよくわからないが、中性付近では炭酸水素マグネシウムができ、これが水に溶けやすいからだと思う。
そしてもう一点は、塩化アンモニウムと同様、炭酸カルシウムの沈殿が生じているところに塩化マグネシウムを加えると沈殿が溶解することを確かめたからである。
その他は前回の条件と同様にして、次のような実験だ。
実験 5 寒天 0.5% ゲル
実験 6 寒天 0.3% ゲル
実験 7 寒天0.1%+ゼラチン2% ゲル
実験 8 イナアガーA 2% ゲル
写真を見ればもう説明はいらない。
まず、結晶は球晶が主だということ。
小さいこと。
ゲルとの関連からいえば、結晶は小さいものの、大きさの傾向は前回と同様だった。
結論から言えば、大きな結晶を作るためにやったことだが、より小さな結晶を作ってしまったということだ。
まあ、思いつきが見事に外れたの巻だ。
まあ自分の傾向として、思いつきの時は、いい着想だと自賛してわくわくし、その結果が楽しみで外れのことなんかあまり考えないのだが、外れがわかると何でこんなことしたんかとがっかりし、もう見るのもイヤになる。
しかし、外れでもまとめることはしないといかん。
誰が読んでくれてるかは知らんが、ブログはそのモチベーションにはなる。
2016-02-06 21:21
トラックバック(0)